Skillnad mellan bensen och fenyl
 Share
Share
Huvudskillnad - Bensen vs fenyl
Aromatiska föreningar är föreningar som har ringstrukturer som består av alternerande enkel- och dubbelbindningar i den ringen. De flesta aromatiska föreningarna består av bensenringar. Fenyl är ett derivat av bensen. Huvudskillnaden mellan bensen och fenyl är det bensen består av sex väteatomer medan fenyl består av fem väteatomer.
Viktiga områden som omfattas
1. Vad är bensen
- Definition, struktur, egenskaper, applikationer
2. Vad är fenyl
- Definition, struktur, egenskaper, applikationer
3. Vad är likheterna mellan bensen och fenyl
- Översikt över gemensamma funktioner
4. Vad är skillnaden mellan bensen och fenyl
- Jämförelse av viktiga skillnader
Viktiga termer: Aromatiska föreningar, Bensen, Elektrofil, Nukleofil, Fenol, Fenyl

Vad är bensen
Bensen är ett färglöst, flyktigt, flytande kolväte närvarande i petroleum. Det är en ringstruktur. De kemisk formel för bensen är C6H6. Alla kolatomer är bundna med varandra genom tre enkelbindningar och tre dubbelbindningar som är anordnade på ett alternerande sätt. De sex väteatomerna är fästa vid de sex kolatomerna, en per varje kol. På grund av närvaron av dubbelbindningar kombineras elektronerna i π-bindningarna tillsammans och bildar två elektronmoln placerat på toppen och botten av bensenringen. Elektronmoln är parallellt med bensenringen. Denna struktur av bensen föreslogs först av Kekule (1872), så det kallas som Kekule struktur.

Figur 1: Struktur av bensen
Alla kolatomer i bensenringen är sp2 hybridiserade. Även om bindningslängden för C-C-enkelbindning är större än C = C dubbelbindning i allmänhet är alla bindningarna i bensen av samma längd. På grund av bildandet av elektronmoln är bindningslängden av bensen någonstans mellan längden av ett enkelbindning och en dubbelbindning. Bensen är en plan struktur och den kan användas för syntes av många andra avancerade föreningar på grund av dess tillgänglighet för substitutioner på ringen.

Figur 2: Två elektronmoln av bensen
Bensenringen är rik på elektroner. Bensen är sålunda tillräckligt nukleofilt. Därför är den huvudsakliga reaktionen som bensen kan genomgå elektrofil substitution. Bensen kan dela sina elektroner med elektrofiler. Elektrofila komponenter är molekyler som saknar elektroner för att bli stabila.
Vad är fenyl
Fenyl är en grupp som härrör från bensen och den kan kombineras med en annan molekyl. De kemisk formel för fenylgruppen är C6H5. Det är också sammansatt av alternerande dubbelbindningar som samma som i bensenring. Fenylgruppen har en ledig punkt där en väteatom saknas. Därför kan denna grupp fästas i en annan molekyl genom denna punkt. Detta gör fenylgruppen väldigt reaktiv.
Vissa tror att fenylgruppen och bensylgruppen är densamma. Men de är väldigt olika eftersom bensylgruppen har en -CH2- grupp bundet till bensenringen.
Den vanligaste molekylen i vilken fenylgruppen hittas är fenol. Där är fenylgruppen bunden med -OH-grupp.
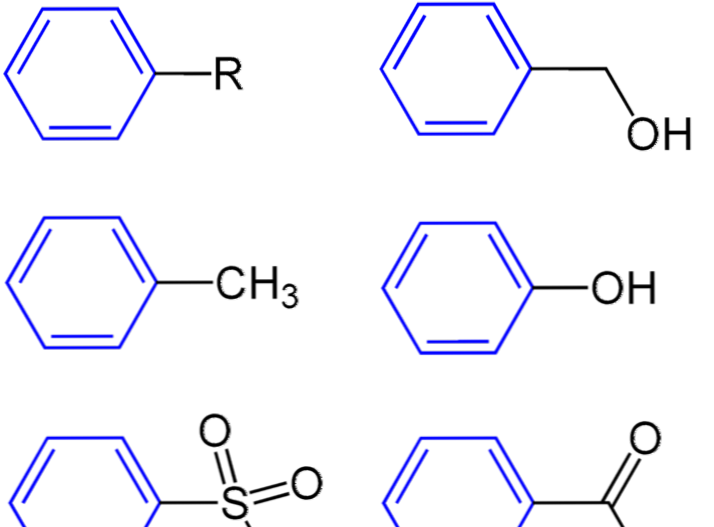
Figur 3: Fenylgrupp (i blå färg)
- Figur 3: Fenylgrupp (i blå färg)
Likheter mellan bensen och fenyl
- Båda molekylerna består av sex kolatomer.
- Båda är ringstrukturer.
- Båda är plana strukturer.
- Hybridisering av kolatom är sp2 i både bensen och fenyl.
- Bondlängden mellan kolatomer är lika (1,4 A0).
Skillnad mellan bensen och fenyl
Definition
Bensen: Bensen är ett färglöst, flyktigt, flytande kolväte närvarande i petroleum.
Fenyl: Fenyl är en grupp som härrör från bensen och den kan kombineras med en annan molekyl.
Antal väteatomer
Bensen: Bensen har sex väteatomer.
Fenyl: Fenyl har fem kolatomer.
Stabilitet
Bensen: Bensen är stabil när den är ensam.
Fenyl: Fenyl är inte stabilt ensam.
Kemisk formel
Bensen: Den kemiska formeln av bensen är C6H6.
Fenyl: Den kemiska formeln för fenyl är C6H5.
Slutsats
Bensen används ofta i syntesen av olika viktiga föreningar. Men försiktighet bör vidtas när man väljer bensen för produkter som har nära relationer till konsumtionen. Det beror på att det har upptäckts att bensen har cancerframkallande effekter. Fenyl är en substituent härledd från bensen. Huvudskillnaden mellan bensen och fenyl är att bensen består av sex väteatomer medan fenyl består av fem väteatomer.
referenser:
1. "Fenylgruppen." Kemi LibreTexts. NP, 21 juli 2016. Web. Tillgänglig här. 21 juni 2017.
2. "Fenyl eller bensyl" Jakt, Ian R. Bensen som substitut. N.p., n.d. Webb. Tillgänglig här. 21 juni 2017.
Image Courtesy:
1. "Bensens strukturella diagram" Av Vladsinger - Egent arbete (Public Domain) via Commons Wikimedia
2. "Fenylgruppens generella formler V" Von Jü - Eigenes Werk (CC0) via Commons Wikimedia
3. "Bensen Quadrupole" Av Michael.hell på engelska Wikipedia (CC BY-SA 3.0) via Commons Wikimedia

